肺癌是最常见的恶性肿瘤之一,目前其发病率及死亡率居高不下,给人们健康带来了巨大威胁。非小细胞性肺癌(NSCLC),作为肺癌比重最高的一种,始终是困扰临床医师的难题,尤其是NSCLC的侵袭和转移,是患者预后不良的重要原因。因此,针对NSCLC侵袭、转移机制的研究成为当前临床医学的重要课题。细胞内的力学调控参与了肿瘤侵袭、转移的各个阶段,细胞膜-细胞骨架连接蛋白ezrin是传递细胞内外力学信号的重要蛋白,炎症微环境中上调的诱导型一氧化氮合成酶(iNOS)水平可介导ezrin蛋白发生亚硝基化(S-nitrosylation,SNO)修饰,从而改变细胞膜与细胞骨架间的力学传递,是非小细胞性肺癌侵袭、转移能力增强的重要物理机制。
近期,南京中医药大学医学与生命科学学院郭军教授团队在生物医学1区杂志《Theranostics》(2017 IF:8.537)上发表研究论文。研究人员通过构建ezrin点突变质粒识别了ezrin的Cys117是其发生SNO修饰的唯一活性位点,而该位点的SNO修饰可增强非小细胞性肺癌的侵袭、转移能力。为了探究非小细胞性肺癌在侵袭、转移过程中ezrin蛋白牵拉张力的变化情况,研究人员进一步构建了基于荧光共振能量转移(FRET)原理的ezrin张力检测探针以及相应的点突变探针,结果显示:ezrin牵拉张力与NSCLC的侵袭、转移能力呈正性相关,而随着ezrin-SNO水平的上调,ezrin牵拉张力呈现增强趋势。更为重要的是,微丝、微管解聚实验以及动力分子抑制实验均证明,向内的微丝张力而不是微管张力是调控ezrin牵拉力的主要力学来源,且ezrin的SNO修饰能促进微丝张力的力学传递作用。
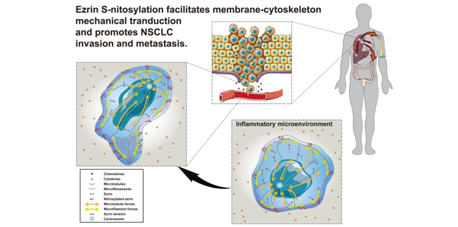
该研究揭示了NSCLC侵袭、转移的细胞内力学调控新机制,探索性地构建了基于细胞骨架结构的亚细胞结构力学作用机制的系统研究模式。同时也阐明了炎症微环境可诱导ezrin的SNO修饰,促进了细胞骨架与细胞膜间的向内力学传递效应,诱导肺癌细胞表面变软,减弱细胞的刚性,使非小细胞肺癌获得更强的侵袭、转移能力。这项研究提示了蛋白质SNO发挥的重要病理作用,为人们重新认识NSCLC发生、发展机制提供了新的视野。
南京中医药大学医学与生命科学学院郭军教授为文章的通讯作者,课题组成员张晓龙和李广明博士为文章的并列第一作者。
全文链接:http://www.thno.org/v09p2555.htm

Xiaolong Zhang, Guangming Li, Yichen Guo, Ying Song, Linlin Chen, Qinli Ruan, Yifan Wang, Lixia Sun, Yunfeng Hu, Jingwen Zhou, Bin Ren, Jun Guo. Regulation of ezrin tension by S-nitrosylation mediates non-small cell lung cancer invasion and metastasis. Theranostics 2019; 9(9):2555-2571. doi:10.7150/thno.32479.